Wprowadzanie do obiegu niebezpiecznego sprzętu medycznego zagrożone jest karą. Ustawa o wyrobach medycznych wprowadziła wymagania dla wytwórców jak też importerów tychże urządzeń. Jakie są to wymagania?
Do sprzętu leczniczego zalicza się przyrządy do diagnozowania, obserwowania stanu zdrowia a także do leczenia. Nie jedynie same urządzenia tj. fotel do dializ ale też oprogramowanie niezbędne do ich obsługi rozpatrywane jest jako przyrząd medyczny. Nieodzowne jest by wszystkie używane narzędzia miały właściwe oznakowania.

Źródło: pixabay.com
Sprzęt medyczny wprowadzony do sprzedaży powinien mieć znak CE. Uzyskanie znaku CE dla urządzenia leczniczego leży po stronie wytwórcy. Nie zwalnia to jednak od odpowiedzialności importera albo też dystrybutora takiego urządzenia jak diatermie chirurgiczne. Dystrybutor jak też importer mają za zadanie zweryfikować, czy wytwórca sprzętu medycznego uskutecznił należytą procedurę oceny zgodności towaru jak też oznaczył przyrząd znakiem CE.
Po wdrożeniu przyrządu na terytorium polski, podmiot, jaki tego dokonał (producent lub importer) ma za zadanie bezzwłocznie powiadomić o tym prezesa Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych oraz Produktów Biobójczych. Podmiot ma na to tydzień od dnia pierwszego wprowadzenia konkretnego przyrządu medycznego na terytorium Polski. Krajowy fabrykant ma obowiązek zameldowania wyrobu na 14 dni przed pierwszym wprowadzeniem do sprzedaży.
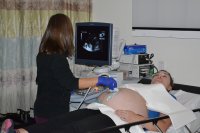
Źródło: http://www.flickr.com
Sprzęt lekarski, jeżeli ma trafić do użytku wprost przez chorego (np. waga niemowlęca), musi mieć instrukcję obsługi w języku polskim. Inaczej jest z odbiorcą profesjonalnym tzn. urządzenie używany w szpitalu nie musi koniecznie mieć instrukcji w języku polskim. Jeśli pomimo posiadania przez sprzęt medyczny certyfikatu CE zagraża on chorym, prezes URPLWMiPB wydaje decyzję o wycofaniu towaru z użycia i obrotu oraz powiadamia o tym Komisję Europejską.
Pod groźbą kary zabronione jest wdrażanie do obrotu jak też używanie produktów medycznych, które wprowadzają w błąd co do własności jak też ról jakie mają spełniać. Wprowadzanie w błąd może następować poprzez fałszywe oznaczenia i błędy w instrukcji obsługi. Więcej na witrynie
